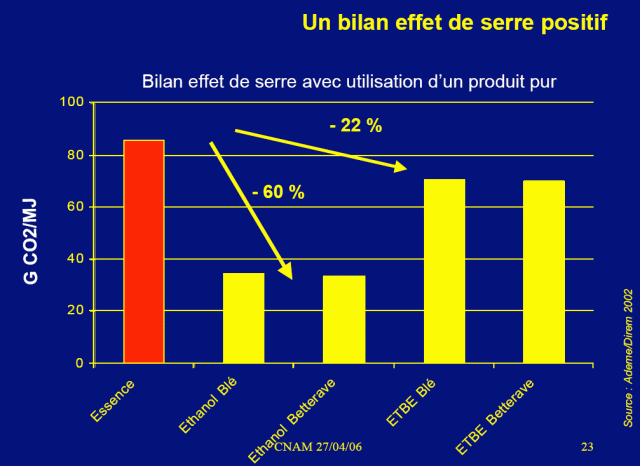
לקבלת תפוקת מנוע שווה, אתנול פולט ולכן 4,56 / 3,55 = פי 1,28 יותר CO2 מאשר בנזין כדי לבצע את אותה עבודה.
במילים אחרות: אתנול פולט 28% יותר CO2 מבנזין.
ואינם נספרים בחישוב זה עבור אתנול:
- עלויות ייצור CO2 של צמח הדגנים או הסוכר
- עלויות זיקוק הצמח לסוכר
- עלויות זיקוק
- עלויות האנרגיה של התסיסה (כלומר ה- CO2 הנפלט לחימום המולסה)
כמה תזכורות לכימיה: סוכר, תסיסה, אלכוהול ו- CO2 ...
נשמור על מסות האטום הבאות המשמשות בסיס לכל החישובים: C = 12 גרם למול, O = 16 גרם למול, H = 1 גרם למול
א) מקרה האלכוהול שהתקבל מתסיסת סוכר
הסוכר המשמש לייצור אתנול הוא ממשפחתו של דיהולוזידים (סוכרוז או מלטוז) בנוסחה: C12H22O11 (ראה http://fr.wikipedia.org/wiki/Sucre#Chimie ) יש מסה טוחנת של 342 גרם אשר על ידי הידרוליזה (היא "צוברת" מולקולת מים), תתן 2 מולקולות של גלוקוז או 2 * C6H12O6 עם מסה טוחנת של 180 גרם למסה כוללת של 360 גרם.
פרטי גלוקוז: http://fr.wikipedia.org/wiki/Glucose
שומת הגלוקוז תסיסה על פי המשוואה:
קוד : לבחור
C6H12O6 --> 2*C2H6O + 2*CO2מוצרים: 2 שומות אלכוהול אתילי (C2H6O = 46 גרם למול) ושתי שומות פחמן דו חמצני (CO2 = 44 גרם למול).
לפני שנשרף ומזניח כל פליטת CO2 אחרת, כל גרם אלכוהול המיוצר ישחרר אפוא במהלך "יצירתו": 44/46 = 0.95 גרם CO2.
וזה לפני בעירתו. במהלך הבעירה של אלכוהול:
קוד : לבחור
C2H6O + 7/2*O2 --> 2*CO2 + 3*H2O או למי שמעדיף מספרים עגולים:
קוד : לבחור
2*C2H6O + 7*O2 --> 4*CO2 + 6*H20שגיאת איזון על ריאגנטים, פעולה מתקנת (שאינה משנה את התוצאות על CO2):
קוד : לבחור
C2H6O + 3*O2 --> 2*CO2 + 3*H2O על ידי שריפה, שומה זו של 46 גרם אלכוהול תייצר לכן 88 גרם CO2 (2 שומות).
זה נותן סה"כ 3 שומות CO2 הנפלטות לשומה של אלכוהול שנשרף: 1 במהלך התסיסה ו -2 במהלך הבעירה. כלומר סך הכל 3x44 = 132 גרם CO2 ל 46 גרם אלכוהול שרוף.
מסקנה: לכן כל גרם אלכוהול פולט במהלך ייצורו ובעירתו לפחות 132/46 = 2,87 גרם CO2.
אני אומר לפחות כי "עמדות CO2 רבות" לא נלקחו בחשבון: ייצור סוכר וזיקוק אלכוהול הם ללא ספק הרעבים ביותר באנרגיה.
ערך זה של 2,87 גרם CO2 / גרם אלכוהול הוא אפוא ערך נמוך מאוד!
ב) מקרה של בנזין (אשר האלכוהול אמור להחליף)
אמשיך בלי לפרט את החישובים בעמוד זה: משוואות בעירה ו- CO2
פליטת CO2 לפחמימנים בפורמולה C2H (2n + 2) = 44n
יישום לבנזין (אוקטן טהור). n = 8
[C8H18] = 8 12 * + = 18 1 114 * g / mol.
מסת CO2 המשוחררת למול אוקטן הנצרך היא: 44 * 8 = 352 גרם.
היחס בין צריכת בנזין לפליטת CO2 הוא 352/114 = 3,09
מסקנה: כל גרם בנזין פולט אפוא 3,09 גרם CO2 במהלך הבעירה
העלות של "זיקוק" להיות, במקרה הרע, 15%, אחד היה להשיג 3.55 גרם CO2 עבור הזיקוק והבערה של בנזין.
ג) השוואת אנרגיה אתנול ובנזין
קוד : לבחור
PCI ethanol = 26 900 kJ/kg
PCI essence = 42 700 kJ/kg
ביעילות המנוע, נדרש לכן 42,7 / 26,9 = יותר ממסה של אתנול כדי לספק את אותה אנרגיה, כלומר פי 1,59.
באיזואנרגיה, לכן יש צורך להוסיף מקדם של 1,59 לפליטת ה- CO2 של אתנול: 2,87 גרם הופכים לכן ל -4,56 גרם. וזכרו: 2,87 גרם אלה כבר הצטמצמו במידה רבה מכיוון שהם לא לקחו בחשבון את גידול הסוכר (אך הספקנים יגידו, ללא סיבה, שבגין בנזין לא לקחנו בחשבון את העלויות של מיצוי והובלה גולמיים)
מסקנה כללית
כדי לספק את אותה כמות אנרגיית הבעירה, פליטת CO2 היא בהתאמה:
- עם בנזין: 3,55 גרם CO2
- עם אתנול: 4,56 גרם CO2
לקבלת תפוקת מנוע שווה, אתנול פולט ולכן 4,56 / 3,55 = פי 1,28 יותר CO2 מאשר בנזין כדי לבצע את אותה עבודה.
במילים אחרות: אתנול פולט 28% יותר CO2 מבנזין.
ואינם נספרים בחישוב זה עבור אתנול:
- עלויות ייצור CO2 של צמח הדגנים או הסוכר
- עלויות זיקוק הצמח לסוכר
- עלויות זיקוק
- עלויות האנרגיה של התסיסה (כלומר ה- CO2 הנפלט לחימום המולסה)
לפיכך אין ספק אפשרי: על פי הנמקה זו, אתנול שמקורו בסוכר חקלאי פולט הרבה יותר CO2 מבנזין. אז איך גופי מדינה ואוניברסיטאות יכולים להשיג הערכות חיוביות כל כך של CO2 על אתנול? הם לא לוקחים תסיסה בחשבון? מה הם חסרים? או, איפה הפגם בהנמקה שלנו?